我国现阶段的创新药之路处于筑底阶段,但已呈现出势不可挡的螺旋上升之势。源头创新、投资并购、License in是现阶段药企补充自身产品管线的主要手段,很多企业都是采用组合拳,三管齐下。
其中,License in具备研发周期短、经验水平积累快、前期研发投入少等诸多优势,是解决未被满足的临床需求的一种快速补充手段,已成为本土企业扩充管线的一种潮流。据火石创造数据库不完全统计,截至2021年5月,已披露的License in交易数量达36起,交易额超1亿美元的有19起,交易数量及金额均有上升之势。
我国创新药之路呈螺旋上升之势
从我国药品发展历史、国家医药/医保政策、地方商保等角度综合分析,国家为创新药发展提供了多方面大力支持,生物制药已具备一定的赛道优势,化学制药随着科学技术的进步也在稳健发展。我国的创新药之路正呈螺旋上升趋势,在不久的将来将实现井喷式发展。
创新药发展的基础是企业具备完善的产品管线,源头创新、投资并购、License in都是药企补充自身产品管线的手段。其中最难的是源头创新,也是我国创新药发展的“卡脖子”环节,License in相较其他两种手段难度最小,风险最低。
我国License in现状
License in,又称许可引进,是通过向产品授权方支付一定首付款,并约定一定金额的里程碑付款及未来的销售提成,从而获得产品在某些国家和地区的开发、生产和销售等商业化权益。License in模式可总结为:首付+里程碑+未来销售提成。其本质是分工合作,即不同企业布局不同的研发阶段,在资金、技术等方面通力合作,实现风险共担、收益共享。
根据火石创造数据库统计,在2015年之后,发生License in交易的企业达62家,其中License in交易数量大于5起的企业有5家,分别为再鼎医药、云顶新耀、百济神州、天境生物、华东医药,通过精准License in入场较早的企业已陆续进入收获期。
表1:2015年后License in交易数量大于5起的企业列表
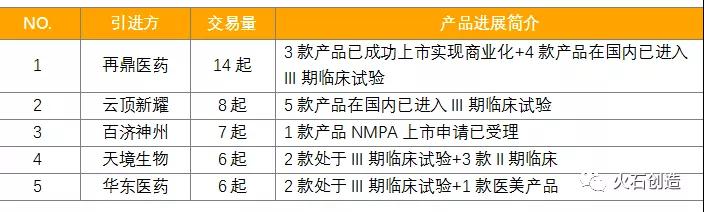
来源:火石创造数据库
再鼎医药专注未被满足的临床需求领域以及通过License in引进差异化的研发管线,其License in的14起交易中,3款产品已成功上市实现商业化,分别为尼拉帕利、肿瘤电场治疗爱普盾、瑞派替尼片;4款产品在国内已进入III期临床试验(包含美国FDA已上市/已向国家药监局递交上市申请的Omadacycline)。
云顶新耀主要布局肿瘤、免疫、心肾以及感染性疾病4个领域,涉及的8款产品均是通过License in获取,其中5款产品在国内已进入III期临床试验(含License in后在美国FDA成功上市的2款产品,分别为Sacituzumab govitecan-hziy、Eravacycline)。
百济神州2020年1月13日License in司妥昔单抗,国家药监局于2021年1月25日受理注射用司妥昔单抗的上市许可申请(BLA)并纳入优先审评。
License in的产品主要包含药品、技术、平台和设备,其中94%为药品的相关权益。适应症主要集中在肿瘤、感染、神经系统、内分泌、眼科等领域。
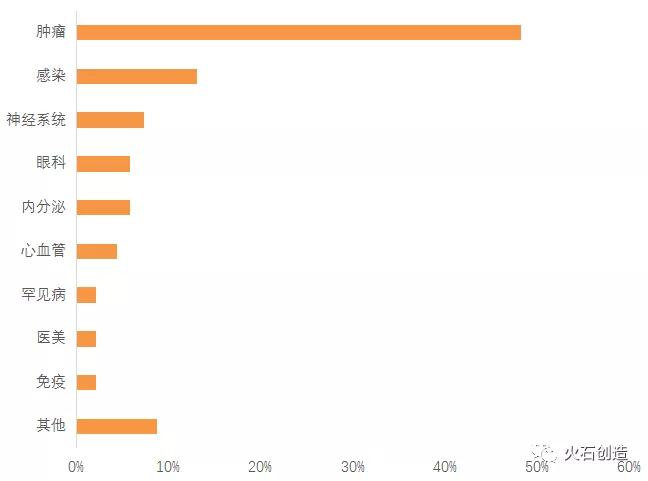
图1:License in适应症分布
来源:火石创造数据库
截至目前,License in的交易量、交易额呈攀升趋势。根据火石创造数据库不完全统计,2019年至今,License in交易额超1亿美元的交易事件达47起,详情见下表。
表2:2019年至今License in交易额超1亿美元交易列表(金额包含已披露的首付款+里程碑付款+销售提成,下同)
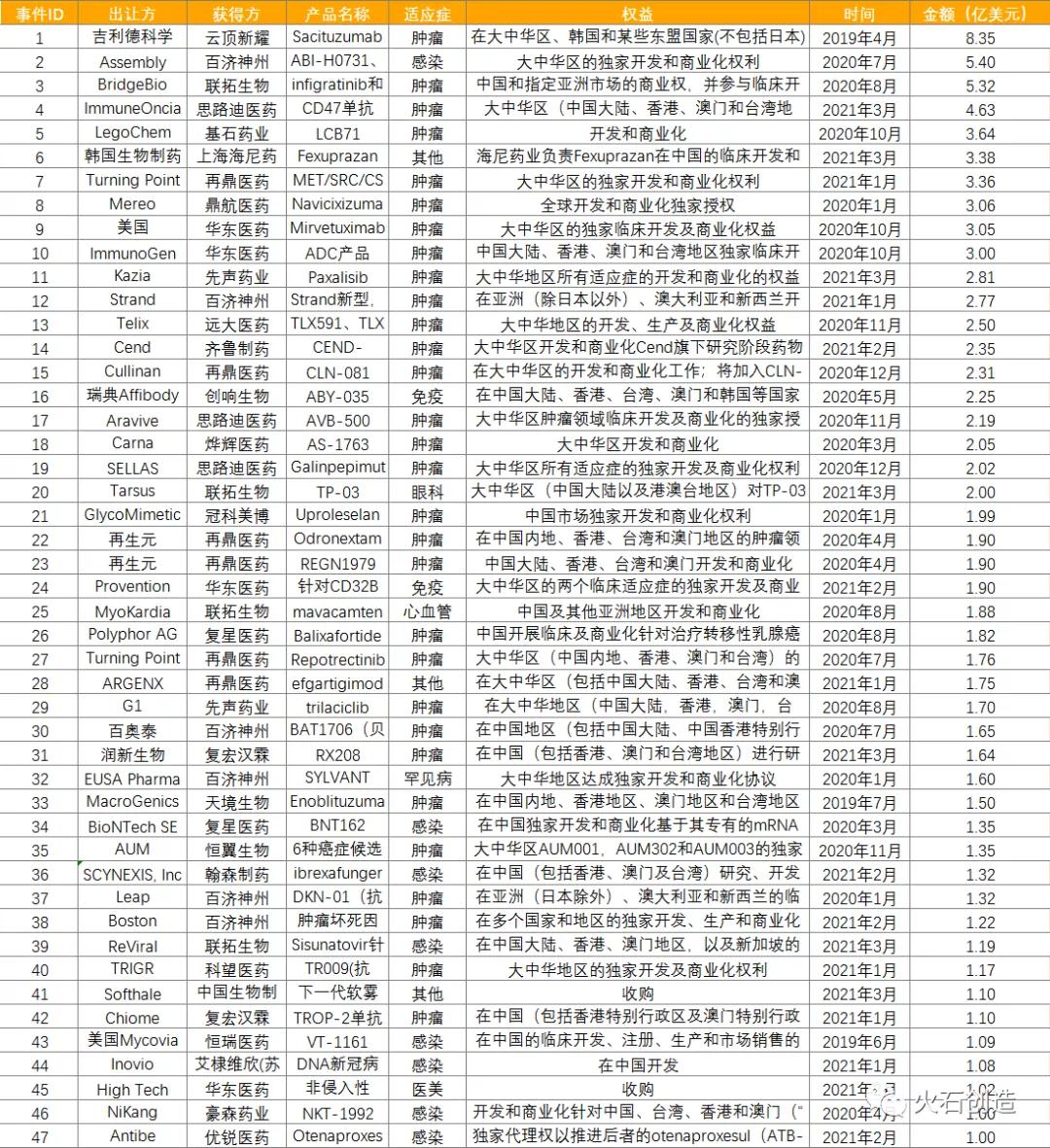
来源:火石创造数据库
另外,2019年全年License in交易额超5亿美元的交易事件为1起,2020年全年License in交易额超过5亿美元的交易事件为2起,2021年暂未出现超过5亿美元的License in交易。
表3:2019年至今License in药品交易总额超过5亿美元列表
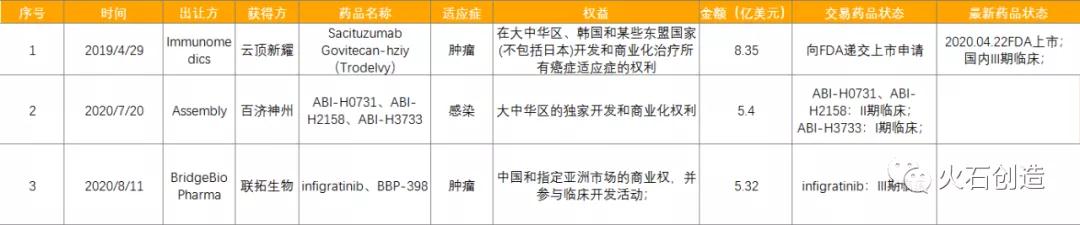
来源:火石创造数据库
License in的能力要求
企业通过License in扩充自身管线需要具备哪些能力呢?
首先是调研能力。目标产品在符合公司战略需求的同时尽可能保持管线的差异化优势,这需要团队有高于行业平均水平的专业科研能力,高度甄别出适合自己企业的好项目。
其次是资金能力与商务能力。License in全周期需要充足的资金,成本的把控、谈判、后续的商业化能力是企业实力的另一项表现。
最后是研发能力与执行能力。License in的项目快速获得阶段成果,需要设计合理的临床试验方案,推进临床试验顺利开展,直至商业化,这需要企业具备高效的研发能力与执行能力。
目前,通过精准的License in,入场较早的企业已陆续进入收获期。但是随着License in市场的逐渐拥挤,交易额水涨船高,且权益的分配导致项目的市场有限,对商业资本来说吸引力可能会逐渐下降,反成为限制License in模式的一大劣势。